产品资质
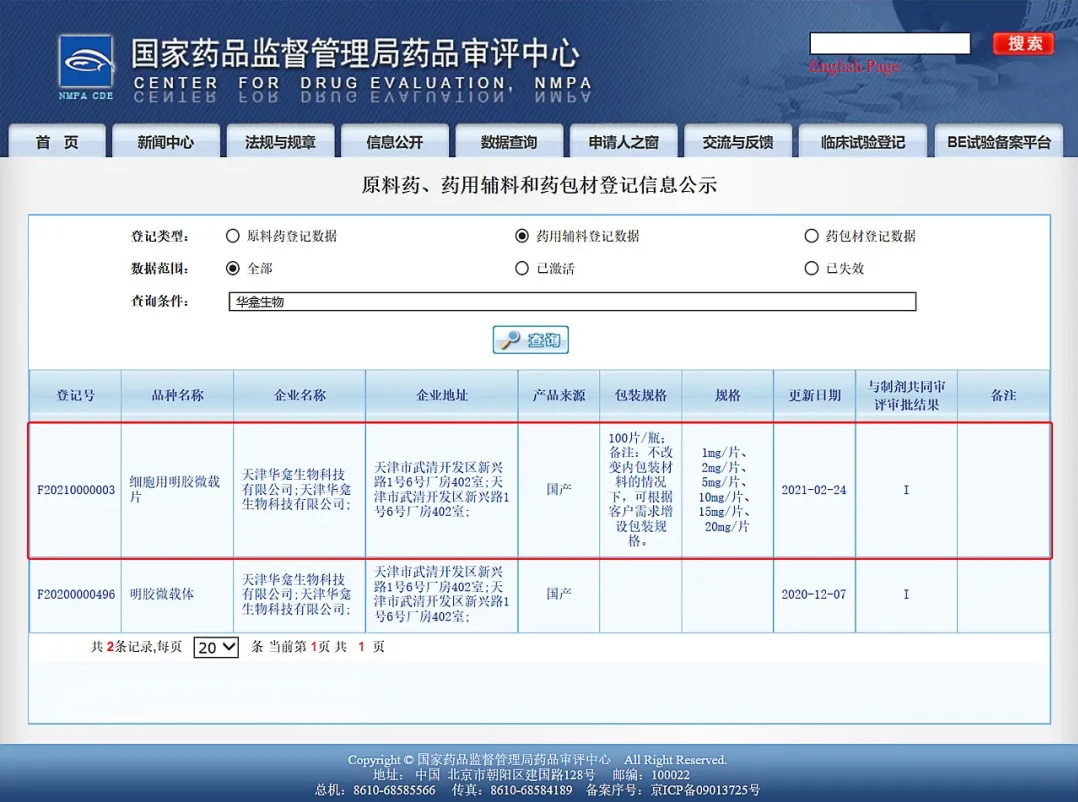
微载体产品完成2项CDE药用辅料备案
华龛生物自主研发的3D微载体,“明胶微载体”及“细胞用明胶微载片”分别于2020年12月7日及2021年2月24日通过国家药品监督管理局药品审评中心(CDE)药用辅料资质备案(登记号:F20200000496、F20210000003)并获得批准,该产品为国内首款可用于细胞药物开发的药用微载体。
完成1项FDA药用辅料DMF备案
2021年4月15日,根据美国FDA官网公示,华龛生物(CYTONICHE)国内首款用于细胞药物生产制备及再生治疗的“细胞用明胶微载片” (GELATIN MICROCARRIER TABLET FOR CELLS, STERILE, EXCIPIENT)完成DMF药用辅料资质备案(DMF:035481),同时也是美国FDA官网公示的DMF备案列表中一款微载体产品。


微载体产品完成1项DMF Ⅱ型资质备案
2023年7月,华龛生物核心原研产品3D TableTrix® 微载体,成功获得FDA下属CDER中心签发的DMF Ⅱ型资质备案,备案号:037798。
此次再获FDA - DMF Ⅱ型资质备案,标志着华龛生物3D TableTrix® 微载体不仅可作为“沉默却极其重要的大多数”—药用辅料,更可作为原料药,成为药物中最主要的有效成分,为疾病的诊断,治疗,减缓,处置或预防以及影响人体的结构和功能等方面发挥药理作用或其他的直接效应。
微载体产品完成1项FDA-MF资质备案
2023年7月,继取得DMF II & Ⅳ型资质备案之后,华龛生物3D TableTrix® 微载体再获美国食品药品监督管理局(FDA)下属生物制剂评价与研究中心(CBER)签发的【MF资质备案】,MF备案号:29721。
此次获得FDA CBER签发备案,是对华龛生物微载体质量控制和生产能力的认可,标志着华龛生物3D TableTrix® 微载体已经达到了更加精细化、更强指向性的生物制品相关国际标准和监管要求,能够稳定、可靠的应用于疫苗及生物制剂生产。


培养基完成1项FDA-DMF资质备案
2023年6月,华龛生物原研产品3D FloTrix® 间充质干细胞无血清培养基获得美国食品药品监督管理局(FDA)DMF备案,DMF备案号:038476。
DMF备案的意义和重要性在于为制药企业提供了向监管机构证明产品品质和安全性的可靠平台,也为监管机构提供了监督和审查药品的途径。
获得DMF备案是3D FloTrix® 间充质干细胞无血清培养基取得的又一重要资质,证明华龛生物的生产工艺和品质控制体系已经达到了国际标准和监管要求。
华龛生物3D微载体全封闭规模化制备的人脐带间充质干细胞获中检院权威认证!
2023年9月6日,由北京华龛生物科技有限公司CDMO平台合作服务的医疗机构送检,采用华龛生物三维细胞培养工艺(3D TableTrix® 微载体+大体系3D FloTrix® vivaSIPIN生物反应器)全封闭规模化制备的人脐带间充质干细胞,经中国食品药品检定研究院质量复核,正式获得其颁发的《检验报告》(编号:SH202311161),成为国内首例通过中检院质量复核的基于3D微载体培养的人间充质干细胞。(此前,华龛生物3D TableTrix® 微载体也已通过中检院相关质量评价及安全性评价。)


华龛生物【3D FloTrix® 百亿工艺】制备的人脐带间充质干细胞再获权威第三方质量认证
2023年9月7日,由北京华龛生物科技有限公司受CDMO客户委托,将采用华龛生物3D FloTrix® 百亿工艺制备的人脐带间充质干细胞,送至武汉珈创生物技术股份有限公司进行质量复核,并正式获得其颁发的《检测报告》(编号:检字<2023>012302052 号)。成为国内首例,通过第三方质量复核的经连续、封闭式生产工艺,单批次制备百亿量级的人脐带间充质干细胞。
科技成果
-
80
个申请80个中国专利
-
17
个申请17个国际专利
-
2
项完成2项CDE药用辅料备案
-
4
项完成4项FDA资质备案
-
2
项完成2项一类医疗器械备案
-
31
篇发表31余篇SCI文章
-
1
项入选1项中关村颠覆性技术研发和成果转化项目
获得ISO9001质量管理体系认证
获得ISO13485医疗器械质量管理体系认证
质量安全

获得ISO9001质量管理体系认证及ISO13485医疗器械质量管理体系认证
华龛生物秉承为客户提供高质量产品的理念,高度重视产品质量,生产平台设计建造符合GMP及ISO相关规定。质量管理体系遵循GMP和ISO运行,较大限度避免过程中污染、差错和混淆的发生,保证产品的安全有效。
中检院和江苏省药物安评
华龛生物的微载体材料及裂解液已完成了第三方机构(中国食品药品检定研究院、江苏省药物安全性评价中心)系列安全性评价实验并形成总结报告。在此基础上,与中国食品药品检定研究院共同建立了检测微载体原料中特异氨基酸及裂解液中酶活性的残留物检测方法及标准。


-
电话
- 服务热线400-012 6688
-
E-mail
- E-mailmarketing@cytoniche.com
- TOP
 京公网安备 11010802037749号
京公网安备 11010802037749号