以下文章来源于外泌体之家(公众号)
细胞外囊泡(EVs)是细胞在病理和生理条件下释放的介导细胞间通讯的物质,而小型EV(sEV,<100-200 nm,即外泌体)的性质和功能与大中型EV(bEVs,>200 nm,即微囊泡)的比较研究较少。来自中国台湾原子与分子科学研究所的研究团队发现,bEV和sEV在三阴性乳腺癌体内的生物分布、诱导肿瘤发生能力不同,并与EV表面膜蛋白的表达密切相关。这些发现对bEV和sEV介导的细胞-细胞通信在癌症发展和治疗中具有重要意义。相关内容以“Membrane Protein Modification Modulates Big and Small Extracellular Vesicle Biodistribution and Tumorigenic Potential in Breast Cancers in vivo”为题发表于1月6日的Advanced Materials杂志上。
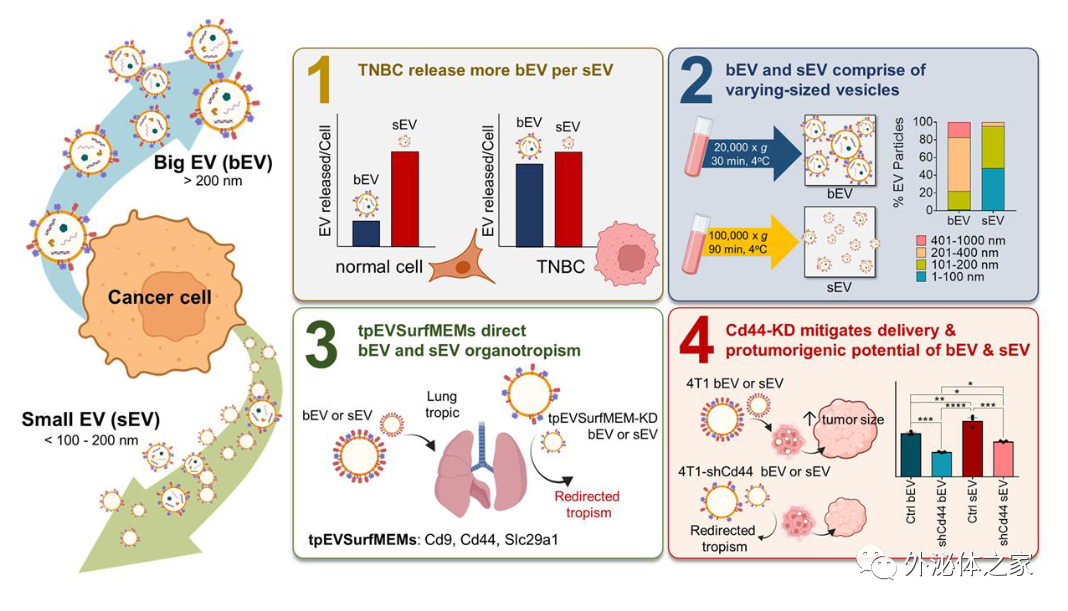
细胞外囊泡(EVs)是由多种细胞释放的具有脂质双分子层的纳米囊泡,介导细胞与细胞之间的通信。小EV(sEV)的直径小于100 - 200纳米,而中型或大型EV(bEV)的直径大于200纳米。与微泡和外泌体不同,bEV和sEV的亚细胞起源是不确定的。另外,细胞还会释放出具有明显货物特征的非膜性纳米颗粒(<50纳米)的exomeres和supermeres。此外,侵袭性肿瘤细胞还会释放含有癌蛋白的大型癌小体(oncosomes,1-10 μm)。
乳腺癌是一种高度异质性的疾病,具有多种临床特征和分子亚型。在乳腺癌亚型中,缺乏雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2 (HER2)的三阴性乳腺癌(TNBC)预后最差,其次是HER2+、luminal B和luminal A亚型。肿瘤EV及其传递的生物活性物质在肿瘤进展中非常重要,包括肿瘤生长、血管生成和转移。然而,大多数乳腺癌EV研究都集中在sEV上,很少有研究系统地探讨乳腺癌中的bEV,并比较其体内性质和功能。此外,乳腺癌亚型是否释放特定EV亚型(bEV和sEV)的差异丰度在很大程度上仍未被探索。
由于EV的大小限制,在体内追踪EV仍然很困难,EV通常需要标记以便后续检测,特别是在体内。EV的追踪一般通过标记EV膜来发挥作用,它依赖于EV表面特性来产生最佳的标记、覆盖范围和信号强度。亲脂性染料标记物(PKH26, DiD, DiR)通常需要标记的时间很短,但会形成纳米束,产生假阳性信号。此外,PKH26和DiR最初用于细胞示踪,其体内半衰期为5 ~ >100天,这可能不能反映标记EV的真实时空特性。与此同时,高剂量标记EV (~ 50-100 μg)通常用于小鼠模型,这不太可能对应于人生理相关的EV剂量。为了避免这些潜在的缺陷,研究团队开发了一种基于生物发光共振能量转移(BRET)的EV报告器(PalmGRET),以实现EV的多分辨率成像和敏感的生物分布分析。
正如已经报告的那样,表面膜蛋白可以在体内动力学中决定EV性质。具体地说,EV表面表达的蛋白质(如四次跨膜蛋白、半乳糖凝集素和整合素)使EV能够与特定受体细胞上的膜蛋白相互作用,从而实现后续生物活性货物的进入和传递。bEV和sEV被发现表达了与其起源细胞相对应的表面膜蛋白。然而,这些膜蛋白在bEV和sEV中的表达程度以及它如何影响它们的生物分布在很大程度上仍然未知,因此需要详细的探索。
在这项研究中,研究团队检测了不同乳腺癌亚型的bEV和sEV释放能力,并系统地比较了EV标记方式、剂量和安全性。研究人员确定了bEV和sEV是不同的EV群体,并确定在侵袭性TNBC亚型中,bEV以更大的bEV:sEV比例释放。基于PalmGRET,研究人员揭示了与亲脂性荧光染料相比,在非致死和生理EV剂量下,EV生物分布的剂量依赖性。值得注意的是,bEVs和sEVs表现出独特的生物分布特征,分别促进了同基因免疫活性TNBC小鼠模型体内肿瘤的生长。通过bEV和sEV质谱,研究人员鉴定了肿瘤进展相关EV表面膜蛋白(tpEVSurfMEMs),包括SLC29A1、CD9和CD44。tpEVSurfMEM的消耗减弱了EV肺转移的器官倾向性,改变了生物分布,并降低致癌潜能。本研究鉴定了bEV和sEV在乳腺癌中的不同体内性质和功能,表明bEV在疾病、诊断和治疗应用中具有重要作用。
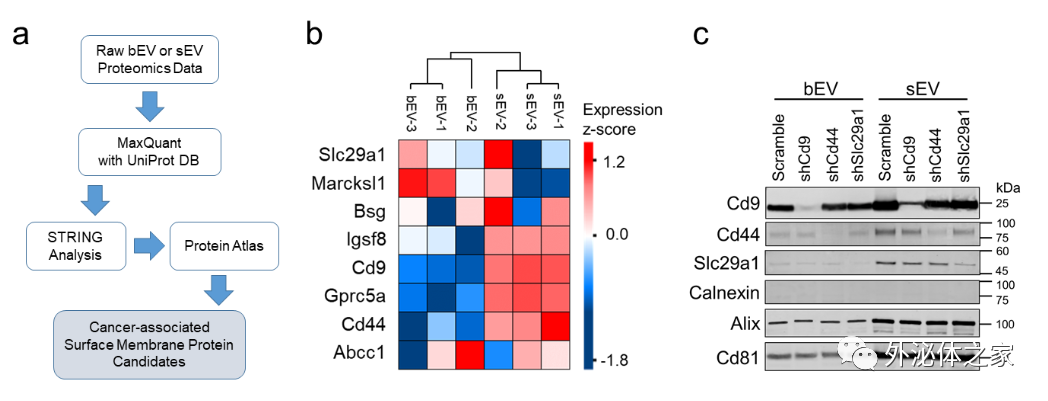
图:通过质谱和WB识别了bEV和sEV中特定表达的膜蛋白谱。
参考文献:
Membrane Protein Modification Modulates Big and Small Extracellular Vesicle Biodistribution and Tumorigenic Potential in Breast Cancers in vivo. Adv Mater. 2023 Jan 6:e2208966.
【华龛生物】
北京华龛生物科技有限公司由清华大学医学院杜亚楠教授科研团队领衔创建,清华大学参股共建。核心技术源于清华大学的科技成果转化。公司专注于打造原创3D细胞“智造”平台,提供基于3D微载体的细胞规模化定制化扩增工艺整体解决方案。
华龛生物核心产品3D TableTrix®微载体(片剂),是自主创新型、首款可用于细胞药物开发的药用辅料级微载体。已通过中检院等相关权威机构的检验报告,并获得2项国家药监局药用辅料资质(CDE审批登记号:F20210000003、F20200000496)。同时,产品获得美国FDA DMF药用辅料资质(DMF:35481)。
华龛生物的产品与服务,可广泛应用于基因与细胞治疗、细胞外囊泡、疫苗及蛋白产品等生产的上游工艺开发。同时,在再生医学、类器官与食品科技(细胞培养肉等)领域也具有广泛应用前景。
公司拥有5000余平米的研发与转化平台,其中包括1000余平的以3D细胞智造及微组织再生医学治疗产品为核心的CDMO服务平台;还拥有4000平米的GMP生产平台,并新建1200L微载体生产线。相关技术已获得100余项专利成果,30余篇国际期刊报道。核心技术项目已获得多项国家级立项支持与应用。

扫二维码用手机看
推荐新闻
-
电话
- 服务热线400-012 6688
-
E-mail
- E-mailmarketing@cytoniche.com
- TOP
 京公网安备 11010802037749号
京公网安备 11010802037749号



